PCR在分子克隆和DNA分析中有多種用途,下面就向大家介紹PCR實(shí)驗(yàn)方法步驟:
方法
1:在冰浴中,按以下次序?qū)⒏鞒煞旨尤胍粺o(wú)菌0.5ml離心管中。
10×PCR buffer
5 μl dNTP mix (2mM)
4 μl 引物1(10pM)
2 μl 引物2(10pM)
2 μl Taq酶 (2U/μl)
1 μl DNA模板(50ng-1μg/μl)
1 μl 加ddH2O至 50 μl
產(chǎn)品名稱 | 規(guī)格 | 貨號(hào) |
5(6)-羧基熒光素(混合物) | 100 mg/1 g/5 g | BJP1211 |
熒光定量PCR原理:
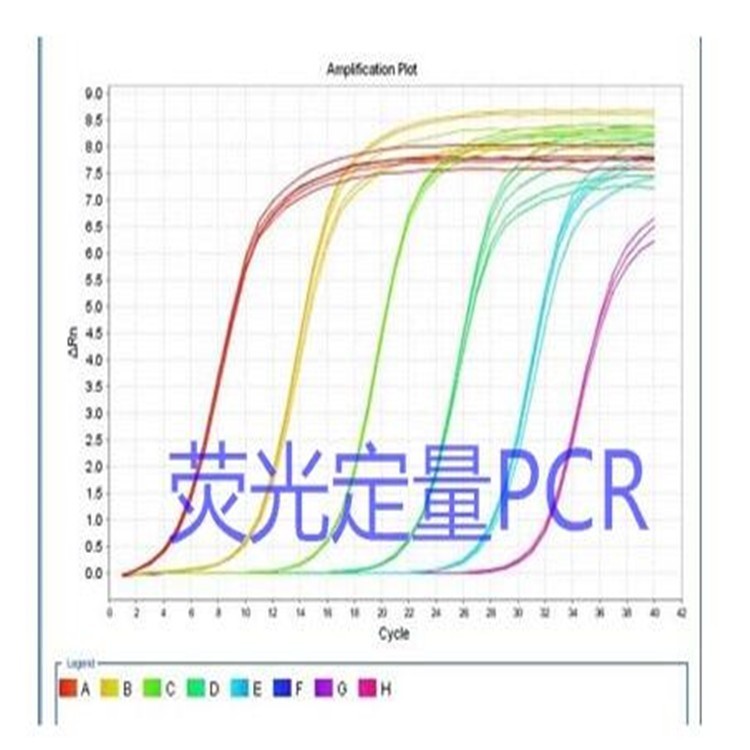
產(chǎn)品僅用于科研熒光定量PCR早稱TaqMan PCR,后來(lái)也叫Real-Time PCR,是美國(guó)PE(Perkin Elmer)公司1995年研制出來(lái)的一種新的核酸定量技術(shù)。該技術(shù)是在常規(guī)PCR基礎(chǔ)上加入熒光標(biāo)記探針或相應(yīng)的熒光染料來(lái)實(shí)現(xiàn)其定量功能的。其原理:隨著PCR反應(yīng)的進(jìn)行,PCR反應(yīng)產(chǎn)物不斷累計(jì),熒光信號(hào)強(qiáng)度也等比例增加。每經(jīng)過(guò)一個(gè)循環(huán),收集一個(gè)熒光強(qiáng)度信號(hào),這樣我們就可以通過(guò)熒光強(qiáng)度變化監(jiān)測(cè)產(chǎn)物量的變化,從而得到一條熒光擴(kuò)增曲線圖。
一般而言,熒光擴(kuò)增曲線可以分成三個(gè)階段:熒光背景信號(hào)階段,熒光信號(hào)指數(shù)擴(kuò)增階段和平臺(tái)期。在熒光背景信號(hào)階段,擴(kuò)增的熒光信號(hào)被熒光背景信號(hào)所掩蓋,無(wú)法判斷產(chǎn)物量的變化。而在平臺(tái)期,擴(kuò)增產(chǎn)物已不再呈指數(shù)級(jí)的增加,PCR 的終產(chǎn)物量與起始模板量之間沒(méi)有線性關(guān)系,根據(jù)終的 PCR 產(chǎn)物量也不能計(jì)算出起始 DNA 拷貝數(shù)。只有在熒光信號(hào)指數(shù)擴(kuò)增階段, PCR產(chǎn)物量的對(duì)數(shù)值與起始模板量之間存在線性關(guān)系,我們可以選擇在這個(gè)階段進(jìn)行定量分析。為了定量和比較的方便,在實(shí)時(shí)熒光定量 PCR 技術(shù)中引入了兩個(gè)非常重要的概念:熒光閾值和 CT值。
 ?
?
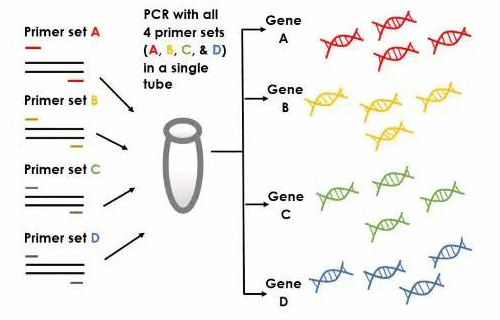
實(shí)時(shí)熒光定量PCR:
實(shí)時(shí)熒光定量PCR技術(shù)有效地解決了傳統(tǒng)定量只能終點(diǎn)檢測(cè)的局限,實(shí)現(xiàn)了每一輪循環(huán)均檢測(cè)一次熒光信號(hào)的強(qiáng)度,并記錄在電腦軟件之中,通過(guò)對(duì)每個(gè)樣品Ct值的計(jì)算,根據(jù)標(biāo)準(zhǔn)曲線獲得定量結(jié)果。因此,實(shí)時(shí)熒光定量PCR無(wú)需內(nèi)標(biāo)是建立在兩個(gè)基礎(chǔ)之上的:
1)Ct值的重現(xiàn)性PCR循環(huán)在到達(dá)Ct值所在的循環(huán)數(shù)時(shí),剛剛進(jìn)入真正的指數(shù)擴(kuò)增期(對(duì)數(shù)期),此時(shí)微小誤差尚未放大,因此Ct值的重現(xiàn)性*,即同一模板不同時(shí)間擴(kuò)增或同一時(shí)間不同管內(nèi)擴(kuò)增,得到的Ct值是恒定的。
2)Ct值與起始模板的線性關(guān)系由于Ct值與起始模板的對(duì)數(shù)存在線性關(guān)系,可利用標(biāo)準(zhǔn)曲線對(duì)未知樣品進(jìn)行定量測(cè)定,因此,實(shí)時(shí)熒光定量PCR是一種采用外標(biāo)準(zhǔn)曲線定量的方法。
外標(biāo)準(zhǔn)曲線的定量方法相比內(nèi)標(biāo)法是一種準(zhǔn)確的、值得信賴的科學(xué)方法。利用外標(biāo)準(zhǔn)曲線的實(shí)時(shí)熒光定量PCR是迄今為止定量準(zhǔn)確,重現(xiàn)性的定量方法,已得到*的*,廣泛用于基因表達(dá)研究、轉(zhuǎn)基因研究,藥物療效考核、病原體檢測(cè)等諸多領(lǐng)域。
 ?
?
定量PCR方法:
a、競(jìng)爭(zhēng)法
選擇由突變克隆產(chǎn)生的含有一個(gè)新內(nèi)切位點(diǎn)的外源競(jìng)爭(zhēng)性模板。在同一反應(yīng)管中,待測(cè)樣品與競(jìng)爭(zhēng)模板用同一對(duì)引物同時(shí)擴(kuò)增(其中一個(gè)引物為熒光標(biāo)記)。擴(kuò)增后用內(nèi)切酶消化PCR產(chǎn)物,競(jìng)爭(zhēng)性模板的產(chǎn)物被酶解為兩個(gè)片段,而待測(cè)模板不被酶切,可通過(guò)電泳或高效液相將兩種產(chǎn)物分開(kāi),分別測(cè)定熒光強(qiáng)度,根據(jù)已知模板推測(cè)未知模板的起始拷貝數(shù)。
b、內(nèi)參照法
在不同的PCR反應(yīng)管中加入已定量的內(nèi)標(biāo)和引物,內(nèi)標(biāo)用基因工程方法合成。上游引物用熒光標(biāo)記,下游引物不標(biāo)記。在模板擴(kuò)增的同時(shí),內(nèi)標(biāo)也被擴(kuò)增。在PCR產(chǎn)物中,由于內(nèi)標(biāo)與靶模板的長(zhǎng)度不同,二者的擴(kuò)增產(chǎn)物可用電泳或高效液相分離開(kāi)來(lái),分別測(cè)定其熒光強(qiáng)度,以內(nèi)標(biāo)為對(duì)照定量待檢測(cè)模板。
c、PCR-ELISA法
利用di高辛或生物素等標(biāo)記引物,擴(kuò)增產(chǎn)物被固相板上特異的探針?biāo)Y(jié)合,再加入抗di高辛或生物素酶標(biāo)抗體-辣根過(guò)氧化物酶結(jié)合物,終酶使底物顯色。常規(guī)的PCR-ELISA法只是定性實(shí)驗(yàn),若加入內(nèi)標(biāo),作出標(biāo)準(zhǔn)曲線,也可實(shí)現(xiàn)定量檢測(cè)目的。
CEM/C1(人急性淋巴細(xì)胞白血病細(xì)胞)說(shuō)明書PEN2 Antibody100 ul
HFSF(人胚胎眼鞏膜成纖維細(xì)胞)說(shuō)明書Pim-1 (D8D7Y) Rabbit mAb10 ug
INS-1(大鼠胰島細(xì)胞瘤細(xì)胞)說(shuō)明書Human <sub>His6</sub>Fas Ligand/TNFSF6 (h<sub>His6</sub>FasL)10 ug
KP-N-NS(人腎上腺神經(jīng)母細(xì)胞瘤細(xì)胞(腦轉(zhuǎn)移))報(bào)價(jià)Human <sub>His6</sub>Fas Ligand/TNFSF6 (h<sub>His6</sub>FasL)100 ul
大鼠骨髓基質(zhì)細(xì)胞*培養(yǎng)基現(xiàn)貨供應(yīng)TNFRSF8/CD30 (E4L4I) XP® Rabbit mAb20 ul
DMEM高糖 (不含L-谷氨酰、丙酮酸鈉、Ca2+)報(bào)價(jià)TNFRSF8/CD30 (E4L4I) XP® Rabbit mAb100 ul
8-香葉草氧基補(bǔ)骨脂素7437-55-0價(jià)格Mcl-1 (D35A5) Rabbit mAb20 ul
偽原纖細(xì)薯蕷皂苷637349-03-2實(shí)驗(yàn)方法Mcl-1 (D35A5) Rabbit mAb100 ul
6-姜酚23513-14-6實(shí)驗(yàn)方法Phospho-HNF1α (Ser247) Antibody100 ul
α-常春藤苷35790-95-5實(shí)驗(yàn)方法Fascin (55k-2) Mouse mAb100 ul
大黃素-1-O-葡萄糖苷38840-23-2實(shí)驗(yàn)步驟NKX6.1 (D8O4R) Rabbit mAb100 ul
大蒜素539-86-6實(shí)驗(yàn)步驟Cas9 (<i>S. pyogenes</i>) (D8Y4K) Rabbit mAb (PE Conjugate)100 ul
牛熊去氧膽酸鈉14605-22-2 實(shí)驗(yàn)步驟BRSK2 (D29B6) Rabbit mAb100 ul
(+)兒茶素225937-10-0 *Synaptophysin (D35E4) Rabbit mAb20 ul
甲基橙皮苷11013-97-1 ?*Synaptophysin (D35E4) Rabbit mAb100 ug
科羅索酸4547-24-4實(shí)驗(yàn)步驟Bafilomycin A1100 ul
雷公藤次堿11088-09-8價(jià)格Phospho-c-Jun (Ser63) (54B3) Rabbit mAb (Biotinylated)100 ul
5(6)-羧基熒光素(混合物)Pichia│pastoris斜面培養(yǎng)物安全等級(jí): 1模式菌株: no應(yīng)用領(lǐng)域: 表達(dá)、分泌生產(chǎn)磷脂酶培養(yǎng)基: 0013生長(zhǎng)條件: 25-28℃存儲(chǔ)條件: -80℃冰箱凍結(jié)法;真空冷凍干燥法;礦物油法
Pseudomonas│sp.凍干物安全等級(jí): 1模式菌株: no培養(yǎng)基: 0002生長(zhǎng)條件: 30℃存儲(chǔ)條件: 液氮超低溫凍結(jié)法;真空冷凍干燥法
Clostridium│acetobutylicum凍干物安全等級(jí): 1模式菌株: no應(yīng)用領(lǐng)域: 丙酮丁醇培養(yǎng)基: 0004生長(zhǎng)條件: 35℃存儲(chǔ)條件: 液氮超低溫凍結(jié)法;真空冷凍干燥法
Ustilago│spermophora分離基物: 蝴蝶凍干物安全等級(jí): 1模式菌株: no培養(yǎng)基: 0013生長(zhǎng)條件: 17-25℃存儲(chǔ)條件: 液氮超低溫凍結(jié)法;真空冷凍干燥法
Lactobacillus│plantarum分離基物: 污泥凍干物安全等級(jí): 1模式菌株: no培養(yǎng)基: 6生長(zhǎng)條件: 37℃存儲(chǔ)條件: -80℃冰箱凍結(jié)法;真空冷凍干燥法
方形鹽盒菌種屬: Haloarcula│quadrata凍干物安全等級(jí): 1模式菌株: yes應(yīng)用領(lǐng)域: 模式菌株培養(yǎng)基: 0212生長(zhǎng)條件: 37℃存儲(chǔ)條件: 液氮超低溫凍結(jié)法;真空冷凍干燥法
Saccharomyces│cerevisiae斜面培養(yǎng)物安全等級(jí): 1模式菌株: no應(yīng)用領(lǐng)域: 酒精釀造培養(yǎng)基: CM0077生長(zhǎng)條件: 28℃存儲(chǔ)條件: -80℃冰箱凍結(jié)法
銅綠假單胞菌(綠膿桿菌)種屬: Pseudomonasaeruginosa分離基物: 動(dòng)物房水的瓶子安全等級(jí): 1模式菌株: no應(yīng)用領(lǐng)域: 測(cè)定抗菌防腐劑,紡織品的細(xì)菌耐藥性檢測(cè),藥效試驗(yàn),質(zhì)量控制菌株。培養(yǎng)基: 2、109生長(zhǎng)條件: 37℃
Streptomyces│albus斜面培養(yǎng)物安全等級(jí): 1模式菌株: no培養(yǎng)基: 0012生長(zhǎng)條件: 28℃存儲(chǔ)條件: -80℃冰箱凍結(jié)法;真空冷凍干燥法
實(shí)驗(yàn)過(guò)程:
一、試劑準(zhǔn)備
1. DNA模板
2.對(duì)應(yīng)目的基因的特異引物(在PCR反應(yīng)中,新合成的DNA是要接在一小段序列上才能繼續(xù)按照模板DNA復(fù)制,而不能從無(wú)到有,憑空合成。這一小段序列就是你所要有設(shè)計(jì)的引物。可以是DNA也可以是RNA,一般20多bp,需要根據(jù)你的模板鏈設(shè)計(jì)。因此,擴(kuò)增不同的基因需要設(shè)計(jì)不同的引物)
3.10×PCR Buffer
4.2mM dNTPmix:含dATP、dCTP、dGTP、dTTP各2mM
5.Taq酶
二、操作步驟
1.在冰浴中,按以下次序?qū)⒏鞒煞旨尤胍粺o(wú)菌0.5ml離心管中。
10×PCR buffer 5μl
dNTP mixl 4μl
引物1(10pM) 2μl
引物2(10PM) 2μl
Taq酶(2U/μl) 1μl
DNA模板(50ng-1μg/μl) 1 μl
加ddH2O至 50 μl
視PCR儀有無(wú)熱蓋,不加或添加石蠟油。
2.調(diào)整好反應(yīng)程序。將上述混合液稍加離心,立即置PCR儀上,執(zhí)行擴(kuò)增。一般:在93℃預(yù)變性3-5min,進(jìn)入循環(huán)擴(kuò)增階段:93℃ 40s → 58℃ 30s → 72℃ 60s,循環(huán)30-35次,zui后在72℃ 保溫7min。
3.結(jié)束反應(yīng),PCR產(chǎn)物放置于4℃待電泳檢測(cè)或-20℃長(zhǎng)期保存。
4.PCR的電泳檢測(cè):如在反應(yīng)管中加有石蠟油,需用100μlLuFang進(jìn)行抽提反應(yīng)混合液,以除去石蠟油;否則,直接取5-10μl電泳檢測(cè)。
三、注意事項(xiàng)
1.PCR反應(yīng)應(yīng)該在一個(gè)沒(méi)有DNA污染的干凈環(huán)境中進(jìn)行。設(shè)立一個(gè)的PCR實(shí)驗(yàn)室。
2.純化模板所選用的方法對(duì)污染的風(fēng)險(xiǎn)有極大影響。一般而言,只要能夠得到可靠的結(jié)果,純化的方法越簡(jiǎn)單越好。
3.所有試劑都應(yīng)該沒(méi)有核酸和核酸酶的污染。操作過(guò)程中均應(yīng)戴手套。
4.PCR試劑配制應(yīng)使用zui高質(zhì)量的新鮮雙蒸水,采用0.22μm濾膜過(guò)濾除菌或高壓滅菌。
5.試劑都應(yīng)該以大體積配制,試驗(yàn)一下是否滿意,然后分裝成僅夠一次使用的量?jī)?chǔ)存,從而確保實(shí)驗(yàn)與實(shí)驗(yàn)之間的連續(xù)性。
6.產(chǎn)品僅用于科研試劑或樣品準(zhǔn)備過(guò)程中都要使用一次性滅菌的塑料瓶和管子,玻璃器皿應(yīng)洗滌干凈并高壓滅菌。
7.PCR的樣品應(yīng)在冰浴上化開(kāi),并且要充分混勻。





































